蛋白质液-液相分离(liquid-liquid phase separation, LLPS)介导细胞中多种“无膜细胞器”(membrane-less organelles)的动态组装,无膜细胞器的形成参与到广泛的生命过程中。近年来,越来越多具有不同生物学功能的蛋白质被发现在体外具有LLPS能力。不同蛋白质的LLPS对蛋白质浓度、pH、离子强度、温度、拥挤试剂等多种不同条件高度敏感。如何有效快速的在体外找到驱动蛋白质LLPS的关键因素?以及如何系统的比较不同蛋白质之间LLPS的能力?这些问题尚未得到阐述。同时,蛋白质处在细胞内复杂的环境之中,系统研究翻译后修饰,RNA, 分子伴侣,基因突变等胞内因素如何影响及调控不同蛋白质LLPS也显得尤为重要。
2022年2月12日,中科院上海有机化学研究所生物与化学交叉中心刘聪课题组与上海交通大学Bio-X研究院李丹课题组合作在Cell Reports Physical Science上发表了题为“A high-throughput method for exploring the parameter space of protein liquid-liquid phase separation”的研究成果。该工作首先建立了基于自动点样机器人及高内涵筛选系统的高通量筛选及评估蛋白质相分离能力的分析方法。该方法仅需少量蛋白质样品并拥有快速的筛选能力,能够在体外高效地表征蛋白质LLPS。进一步,运用建立的新方法筛选了近30种不同蛋白质样品,发现不同蛋白普遍具有不同程度的LLPS能力,首次提出蛋白质相分离空间(LLPS space)这一全新概念来刻画并比较蛋白LLPS的能力与性质。进一步,阐释了蛋白质LLPS的能力受蛋白质-蛋白质相互作用、翻译后修饰、基因突变以及分子伴侣的动态调控。本工作为系统高效研究不同蛋白质LLPS提供了有力的新方法,并为理解蛋白质LLPS的性质及动态调控提供了新的视角。
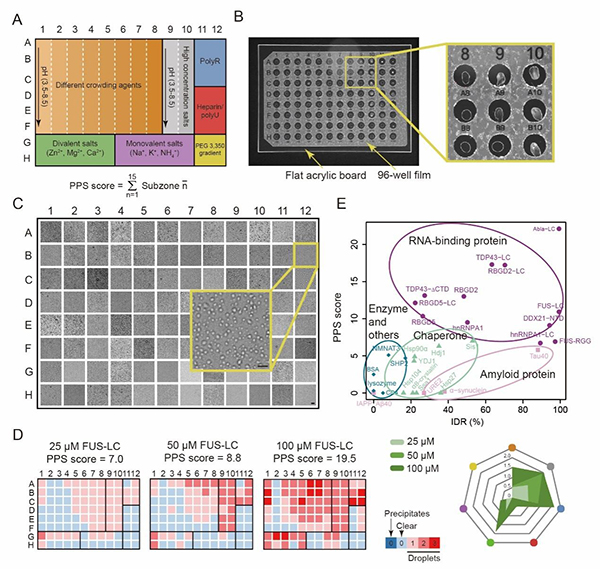
在本工作中,研究者基于已有的文献数据整理并总结了诱导蛋白质发生LLPS的不同条件,并建立了适用于体外筛选的96孔板筛选系统。通过自动点样机器人降低蛋白质样品的使用量,以及结合高内涵筛选系统快速拍摄方法,达到短时间高通量的鉴定不同条件下多个不同蛋白质样品的LLPS (图1)。同时,对筛选结果进行赋值(PPS score),并结合LLPS space来系统比较不同蛋白质系统LLPS的能力。研究者首先通过对已知的相分离蛋白进行筛选验证了96孔板筛选系统的实用性,接下来对近30个不同的蛋白质样品(RNA结合蛋白,淀粉样蛋白,分子伴侣,蛋白酶等)进行筛选,发现并鉴定了各个蛋白质所具备的相分离条件,计算出不同蛋白的LLPS space,并揭示了蛋白质相分离潜在的通用属性(图1)。
图1 高通量蛋白质相分离筛选方法的建立与运用
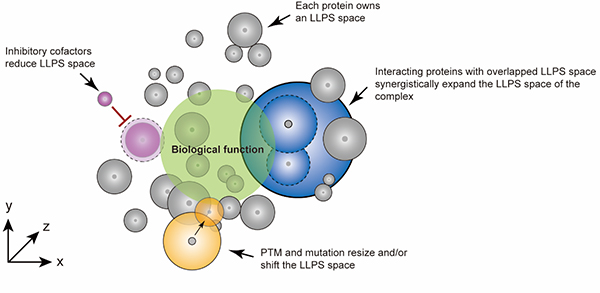
研究者进一步利用高通量的筛选方法对复杂系统的蛋白质LLPS调控进行探究。首先,发现蛋白质之间的相互作用可以极大地降低多组分下蛋白质相分离浓度的阈值,暗示了细胞中各蛋白质在极低浓度下可通过相互作用驱动无膜细胞器形成。其次,发现不同的分子伴侣能够通过与底物蛋白相互作用从而正(负)调控蛋白系统的相分离能力和动态属性。最后,阐释了特定位点翻译后修饰或者遗传突变对蛋白质的LLPS具有重要的调控作用。综上,本研究工作不仅有助于研究者快速探究特定蛋白质相分离能力及其调控机制,同时还有助于我们更加全面系统地认识蛋白质相分离在复杂生命过程中的作用(图2)。
图2 不同蛋白质液-液相分离空间(LLPS space)的表征与动态调控
上述工作由中科院上海有机所生物与化学交叉研究中心刘聪研究员和上海交通大学李丹特别研究员为共同通讯作者,李丹课题组博士研究生李懿臣和刘聪课题组博士谷锦阁为共同第一作者。经费支持主要来自中国科学院,国家自然科学基金委,以及上海市科委的资助。