上海有机所在喹啉类化合物的不对称烯丙基取代反应方面取得重要进展
催化不对称去芳构化(Catalytic asymmetric dearomatization,CADA)反应是近年来兴起的一类重要的不对称合成方法。该类反应以简单易得的芳香化合物为原料,可以快速构建手性螺环或多环化合物。然而由于该类反应需要在破坏底物芳香性的同时实现对立体化学的调控,因此建立合适的反应条件和拓展底物的适用范围是发展该类反应面临的重要挑战。目前研究较多的催化不对称去芳构化反应主要集中于吲哚、吡咯、萘酚、苯酚等富电子芳香化合物。在反应中通常仅涉及破坏一个芳环的芳香性。
中国科学院上海有机化学研究所金属有机化学国家重点实验室游书力研究员团队一直致力于铱催化不对称烯丙基去芳构化反应研究(Acc.Chem. Res.2014,47, 2558)。2014年,他们发现通过在碱性条件下攫取苄位活泼质子的方法,可以使贫电子芳杂环如吡啶、吡嗪作为良好的氮亲核试剂参与不对称烯丙基去芳构化反应(Angew. Chem. Int. Ed.2014,53, 6986)。随后他们又将该策略成功地推广到喹啉、异喹啉、苯并噁唑、苯并噻唑、苯并咪唑等多类含氮芳杂环(J. Am. Chem. Soc.2015,137, 15899; Angew. Chem. Int. Ed.2017,56, 1530)。
最近,该团队又成功地发展了5-羟基喹啉和7-羟基喹啉这两类重要含氮芳杂环的不对称烯丙基取代反应,利用手性三氮唑卡宾的铱络合物为催化剂实现了结构新颖的手性环状烯酮类化合物的高对映选择性合成(J. Am. Chem. Soc.2018,140, 3114)。与以往的研究结果不同,该类反应在形式上实现了对两个连续芳环的芳香性的破坏。通过对反应底物和产物的核独立化学位移(NICS(1)_ZZ)、等化学屏蔽表面(ICSS),以及多中心键级的理论计算,证实该反应使得5-羟基喹啉和7-羟基喹啉的两个芳环的芳香性均显著降低。为进一步发展同时破坏多个连续芳环芳香性的催化不对称去芳构化反应打下良好的基础。同时,该反应具有很强的实用性,可在非惰性气体氛围和未经干燥处理的有机溶剂中进行。利用该反应为关键步骤,研究人员实现了天然产物(-)-gephyrotoxin的高效不对称形式合成。
上述研究工作得到了国家自然科学基金委、科技部、中国科学院战略性先导科技专项(B类)和上海市科委的资助。
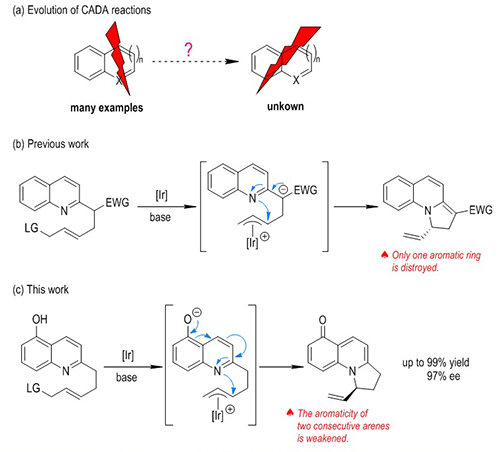
图1 喹啉衍生物的不对称烯丙基取代反应
附件下载: