上海有机所在硫肽类抗生素的生物合成机制研究方面再获重要进展
黄素依赖的加氧酶(Flavin-dependent oxygenase)是一类以黄素腺嘌呤二核苷酸或黄素单核苷酸为辅酶的氧化还原酶,在生命过程的各个阶段广泛参与各种与氧化还原相关的生化反应。近期,中国科学院上海有机化学研究所生命有机化学国家重点实验室刘文研究员课题组和金属有机国家重点实验室郭寅龙研究员课题组进行合作,以硫肽类抗生素的典型代表硫链丝菌素(Thiostrepton,TSR)为研究对象,报道了一例黄素依赖的加氧酶通过底物的立体专一性氧化来促进吲哚五元环的扩环重排,揭示了自然界中一种喹啉单元形成的酶学新机制。相关成果已于8月18日在线发表于《美国化学会志》上(J. Am. Chem. Soc. 2017, DOI: 10.1021/jacs.7b05337)
硫肽类抗生素是一类富含元素硫、结构被高度修饰的环肽类抗生素,大多具有良好的抗菌活性。含喹萘啶酸(Quinoline acid,QA)单元的双环硫肽与众不同——除了抗耐药菌活性外,还被发现具有抗癌、抗疟、抗支原体以及免疫抑制等活性,例如代表性成员硫链丝菌素TSR。刘文课题组长期从事硫肽类抗生素的生物合成机制及分子改造研究,并在前期工作中证实了QA部分的修饰对于硫肽类抗生素的生物活性和理化性质改善十分重要(Chem. Biol. 2015, 22, 1002; Curr. Opin. Biotechnol. 2017)。QA的生物合成起源于L-色氨酸,但如何进过分子内的重排扩环反应形成关键的中间体喹啉酮(quinoline ketone)并不清楚。结合体内生物转化、体外生化验证等多种手段,研究人员发现黄素依赖的加氧酶TsrE能够以还原态黄素FADH2为辅因子,利用O2 立体专一性地氧化中间体2-甲基吲哚-3-丙酮酸并形成C3位为S构型的高活泼性的羟基中间体,从而诱发了包括C-N键的断裂和重新形成紧密偶联在内的水解开环、环化和芳构化反应,促使吲哚转化为喹啉单元;后者经过修饰与活化之后,与来源于前体肽的硫肽核心骨架整合,形成TSR-型双环硫肽成员所特有的侧环体系(Chem. Biol. 2012, 19, 443;ACS Chem. Biol. 2016, 1 1, 2673; Proc. Natl. Acad. Sci. U. S. A. 2016, 113, 14318)。郭寅龙研究员课题组的张芳副研究员运用质谱分析手段,对这一不同寻常的扩环重排过程中产生的高活泼性中间体进行了捕获和鉴定。上述发现代表了色氨酸官能团化的一种新策略,丰富了有关TSR-型双环硫肽侧环构筑的认知,所催化的选择性氧化反应在有机化学合成中具有潜在的应用价值。有趣的是,这种吲哚扩环机制在自然界中可能普遍存在,比如植物来源的抗疟药奎宁(Quinine)类天然产物的形成也经历了类似的选择性氧化诱发的扩环过程。
刘文课题组的博士生林芝为上述研究工作的第一作者。该工作得到了国家自然科学基金委、科技部、上海市科委和中科院等相关项目的资助。
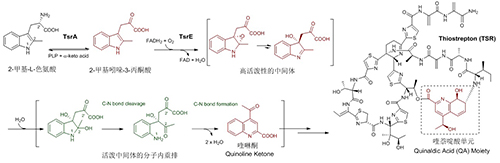
TSR生物合成途径中喹啉单元的形成机制
附件下载: