上海有机所在II型聚酮合酶研究方向取得进展
北京时间2024年11月6日,中国科学院上海有机化学研究所刘文课题组在Nature Synthesis上在线发表了题为“Analysis of siderochelin biosynthesis reveals that a type II polyketide synthase catalyses diketide formation”的研究成果(https://www.nature.com/articles/s44160-024-00677-4)。该工作报道了一类以甲基丙二酰辅酶A为羧基底物(延伸单元)催化二酮单元形成的新型II型聚酮合酶(PKS),在打破了40年来对II型PKSs延伸单元单一性的认知,并丰富了对天然产物和生物学共进化的理解,为聚酮类化合物结构多样性的发展与应用奠定了重要基础。
II型PKSs是多酶复合物,通过催化迭代的脱羧缩合反应形成具有广泛药理学活性的聚酮类天然产物,例如临床上使用的广谱性抗菌药四环素和抗肿瘤药柔红霉素等。1984年,著名的微生物学家David Alan Hopwood教授首次报道了II型聚酮类天然产物放线菌红素的生物合成基因簇(Nature. 1984, 309, 462),从此开启了聚酮类天然产物生物合成的新篇章。直至今日,已知的II型PKSs均严格使用丙二酰辅酶A为延伸单元进行脱羧缩合,导致在聚酮链延伸过程缺乏α-烷基化,极大限制了该类聚酮天然产物的结构多样性。
上海有机所刘文课题组长期从事聚酮、聚肽类天然产物相关的装配线化学的研究,建立了高效、可靠的装配线化学研究方法,并深入揭示装配线上特殊的修饰蛋白招募机制、环化机制、糖苷单元形成机制等新颖的装配线化学(J. Am. Chem. Soc. 2021,143, 19719; J. Am. Chem. Soc. 2022, 144, 14945;J. Am. Chem. Soc. 2023,145, 5017; Nat. Chem.2023, 15, 177)。基于装配线化学的经验积累及前期本课题组报道含有2, 2’-联吡啶结构天然产物caerulomycin(CAE)和collismycin(COL)的生物合成研究(Nature Commucation, 2021, 12, 3124),刘文课题组从CAE和COL中吡啶单元生物合成关键酶CaeP1和CaeP2出发,通过基因组挖掘手段确定吡咯联吡啶类天然产物——络铁菌素(SIDs)的生物合成基因簇,并在其中发现一类特殊的II型PKS。它催化甲基丙二酰辅酶A(延伸单元)与3-羟基吡啶甲酸(3-HPA,起始单元)发生脱羧缩合,合成吡咯环的二酮结构单元。通过基因敲除、同位素喂养及体外生化实验,详细阐明了该II型PKS的催化逻辑:腺苷酰化酶催化3-HPA与ATP的反应生成3-HPA-AMP,由酰基转移酶(AT)催化其上载至酰基载体蛋白(ACP),随后通过硫酯交换反应转移至酮基合成酶(KS),形成3-HPA-S-KS。同一套AT和ACP还负责甲基丙二酰辅酶A的上载,随后KS催化这两个非丙二酰羧基底物的脱羧缩合(图1)。此外,该II型PKS具备强大的底物兼容性和可进化性,可以催化α-烷基化修饰各异的延伸单元和环系各异的启始单元发生脱羧缩合反应,对KS的定向改造则可进一步提高其底物耐受性。
该研究报道了一类以甲基丙二酰辅酶A为延伸单元催化二酮结构形成的新型II型PKS,阐明了其中的催化逻辑,并拓展了该套体系对多种羧基底物的高相容性及对“非天然/不识别”底物的可进化性。该工作不仅丰富了PKSs酶学领域的认知,加速了聚酮类化合物结构多样性的发展与应用,同时也为小分子与生物体共进化理论的推进提供了新的思路。上海有机所刘文团队钱瑶博士,郜仅敏博士(现加利福尼亚大学圣巴巴拉分校博士后)为该论文的共同第一作者,上海有机所刘文研究员为通讯作者。该工作得到国家重点研发计划和国家自然科学基金的支持。
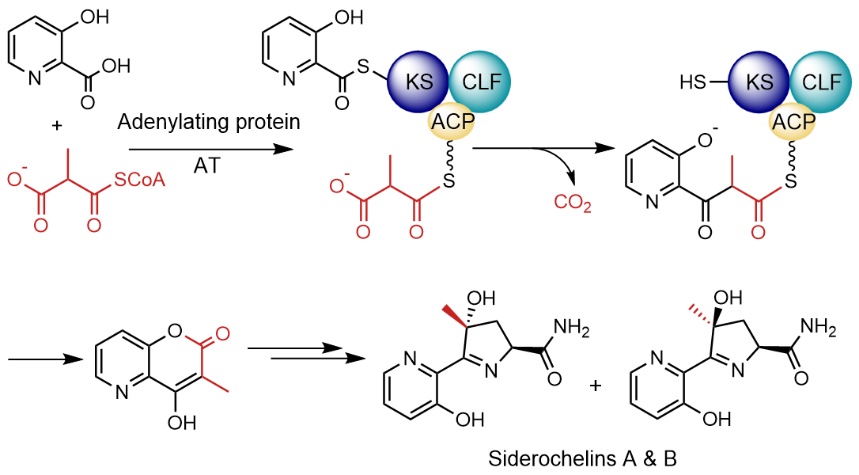
图1 络铁菌素生物合成途径中新型II型聚酮合酶催化的二酮单元形成
附件下载: