烯基硅烷由于其低毒性、高稳定性和易于转化成其他官能团,因此是在有机化学中重要的合成子。最直接的和原子经济性的合成烯基硅烷的方法是金属催化炔烃的硅氢化反应。虽然近些年来金属催化炔烃的硅氢化反应,尤其是利用廉价金属铁、钴等的络合物催化的反应得到很大发展,但仍然存在硅烷中只有一个硅氢键参与反应、反应模式单一等局限性。烯炔分子作为一类特殊的底物,其硅氢化反应的化学、区域和立体选择性的调控具有挑战性。目前,烯炔分子的硅氢化反应局限于炔烃部分,因此,探索烯炔分子中的炔烃和烯烃与硅烷的高选择性反应并构建具有碳手性和硅手性的烯基硅烷化合物的新方法是非常有意义的。
中国科学院上海有机化学研究所金属有机化学国家重点实验室的孟繁柯课题组一直致力于钴催化的不对称反应的研究。在前期的研究中,孟繁柯课题组发展了一系列钴催化新型不对称反应(Angew. Chem. Int. Ed. 2019, 58, 11049 –11053;Angew. Chem. Int. Ed. 2021, 60, 2694–2698;Cell Reports Physical Science 2021, 2, 100406;J. Am. Chem. Soc. 2021, 143, 12755)。近期,该课题组在探索烯炔的不对称硅氢化反应过程中,利用位阻诱导Ojima-Crabtree异构化串联分子内硅氢化的策略,发现通过一级硅烷两个硅氢键与烯炔的炔烃和烯烃依次反应,一步区域和立体选择性的构建含有碳手性中心和硅手性中心的烯基硅烷化合物,取得了新的研究进展。(J. Am. Chem. Soc. 2022, DOI: 10.1021/jacs.2c00288)
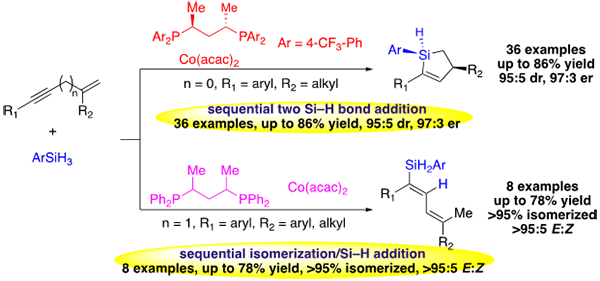
孟繁柯课题组发现,通过原位还原产生一价钴络合物,诱导一级硅烷可以首先与烯炔的炔烃部分发生化学和区域选择性的硅氢化反应,实现一个硅氢键的插入,通过往烯烃上引入位阻,促使烯基钴中间体发生Ojima-Crabtree异构化,从而使得该硅氢化是反式加成,产生的二烯基硅烷中间体中,硅氢键可以进一步在同一手性钴催化剂作用下,发生分子内的区域、非对映和对映选择性的第二次硅氢化反应,一步构建一个碳手性中心和硅手性中心,实现一级硅烷分子中两个硅氢键与一分子烯炔的两个反应位点的精准反应。产物手性烯基硅烷的手性硅氢键可以发生立体专一的转化,合成一系列含有多样性官能团的手性四级硅烷。
此项工作由有机所博士生陆文心同学和中国石油大学(北京)联培硕士生赵永梅同学完成。该研究得到国家自然科学基金委、上海市科委、中国科学院、上海有机所和金属有机化学国家重点实验室的大力资助。
图 钴催化烯炔的区域和立体选择性的串联硅氢化反应