上海有机所交叉中心揭示坏死细胞终末阶段的蛋白切割机制和生理意义
2026年4月7日,中国科学院上海有机化学研究所生物与化学交叉研究中心主任袁钧瑛院士团队在Vita期刊在线发表了题为Distinct necrotic protein cleavages define terminal events in necrosis 的研究论文。该研究在单细胞水平对细胞死亡机制进行了研究,意外发现即使在相同的促细胞死亡条件下,细胞仍可能选择进入凋亡或坏死两种不同的死亡路径,从而将细胞死亡调控的认识提升至单细胞水平。该工作进一步系统探讨了细胞坏死的执行机制,发现传统认知中的细胞坏死执行机制并不足以完成细胞死亡,而坏死的终末阶段依赖胞外蛋白酶的介入,这些蛋白酶介导的大规模且具有特异性的蛋白水解,使坏死细胞中出现类似于凋亡过程中由caspase介导的蛋白切割事件,并在促进坏死细胞清除及抑制自身免疫反应中发挥关键作用。基于上述发现,研究团队进一步开发了可特异性识别坏死相关蛋白切割产物的单克隆抗体,为在病理样本中精准识别和研究坏死细胞提供了全新的分子工具。
坏死细胞膜破裂触发胞外蛋白酶介导的特异性蛋白切割
过去对坏死性细胞死亡的研究,主要聚焦于膜破裂后释放出的损伤相关分子模式(DAMPs)、炎症因子和趋化因子对组织微环境及免疫系统的影响,而较少关注膜破裂之后,组织液或血液中的物质是否会反向进入死亡细胞,并继续参与调控其终末命运。
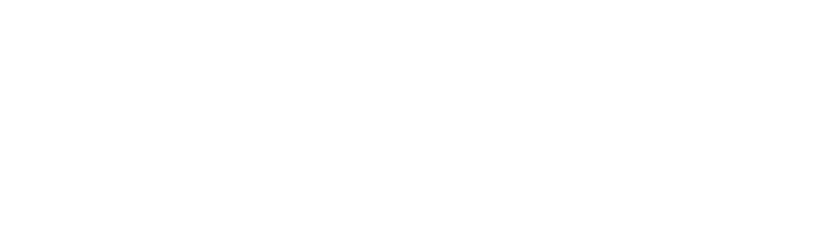
针对这一问题,研究团队发现,在多种坏死性细胞死亡(包括程序性坏死,铁死亡和细胞焦亡)中普遍存在一个共同现象:细胞膜破裂后,原本存在于组织液、血液或细胞外环境中的蛋白酶可进入细胞内部,进而诱导一系列坏死特异性的蛋白切割事件。通过新生N端标记蛋白质质谱(neo-N-terminomic)分析,研究人员系统绘制了坏死细胞的切割位点图谱。结果显示,这些切割主要发生在精氨酸(Arg)和赖氨酸(Lys)残基的碳端,呈现出明显不同于凋亡中caspase切割的位点偏好。
这些切割事件广泛分布于多个细胞区室,包括细胞核、细胞膜、细胞质、高尔基体和内质网等。尽管不同细胞系、不同坏死方式以及不同组织样本间存在一定的异质性,但该研究仍鉴定到一系列在多种条件下保守存在的底物及切割位点。这表明,坏死性蛋白切割并非膜破裂后的随机性降解,而是具有底物偏好和位点选择性的分子事件,提示其可能承担特定的生理功能。
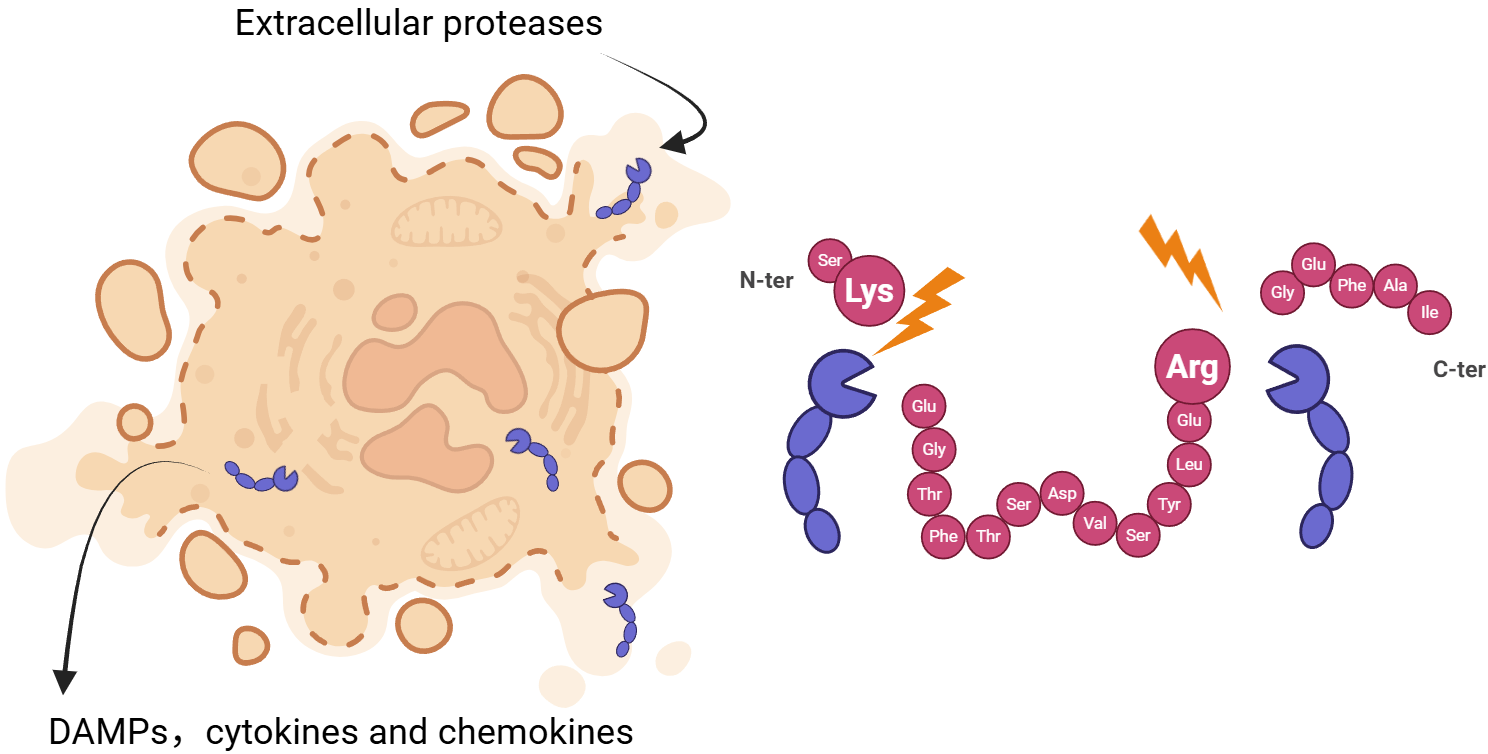
图1. 胞外蛋白酶主要识别并切割精氨酸(Arg)和赖氨酸(Lys)残基
坏死性蛋白切割调控坏死细胞清除与免疫原性
细胞凋亡的发生由caspase家族主导,其特点是细胞膜保持完整,内容物不泄露。凋亡细胞中caspase的激活不仅执行了细胞死亡,同时通过调节磷脂酰丝氨酸(PS)外翻、膜出泡和凋亡小体形成、基因组DNA降解等过程,保证了凋亡细胞的清除与降解。而坏死则以细胞膜完整性丧失为特征,但目前我们仍不清楚坏死细胞具体是如何实现细胞清除的。
该研究发现,使用亮肽素抑制坏死蛋白切割可显著抑制程序性坏死、铁死亡和细胞焦亡过程中细胞基因组DNA的降解。进一步的体外吞噬实验和体内腹腔注射实验表明,当坏死性蛋白切割被抑制后,吞噬细胞对坏死细胞,尤其是对核碎片的清除效率明显下降。更重要的是,这种清除障碍并非单纯影响残骸处理,而会进一步诱发病理后果,使受试小鼠出现针对自身蛋白的抗体升高以及脾肿大等自身免疫相关表型。
这些结果表明,膜破裂后由胞外蛋白酶介导的坏死性切割,并不是坏死后的伴随现象,而是机体高效、安全清除坏死细胞残骸的重要机制。该研究因此将坏死终末阶段从传统意义上的“被动瓦解”,推进为一个具有明确功能意义的主动清理过程。
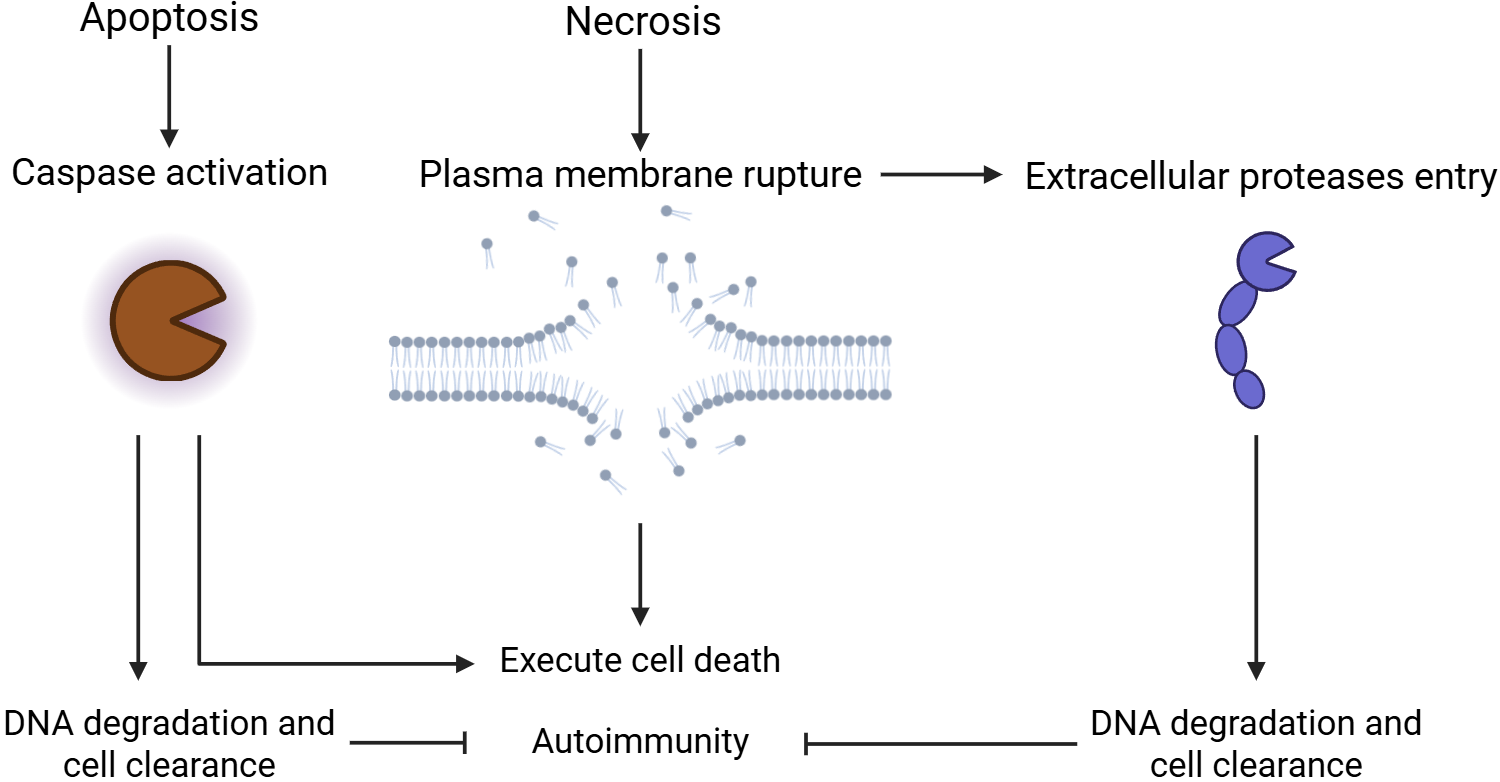
图2. 胞外蛋白酶进入坏死细胞后促进DNA降解与清除,并避免自身免疫反应
单细胞视角揭示细胞死亡方式的异质性与研究新范式
传统细胞死亡研究多基于群体水平分析,即通过整体样本的分子变化来定义某一刺激诱导的死亡方式。然而,这种策略容易掩盖单细胞层面的命运异质性。
该研究团队利用改进的超高分辨率三维光学衍射断层扫描(super resolution optical diffraction tomography, ODT)技术,在单细胞尺度上动态观察细胞死亡进程。研究人员在细胞焦亡模型中发现,即便是在同一刺激条件下,细胞群体内部也并非沿单一路径死亡:一部分细胞表现出经典凋亡样形态,另一部分则表现出GSDMD介导的膜破裂坏死样死亡。与之对应,在分子层面,研究团队同时检测到caspase介导的凋亡性蛋白切割和胞外蛋白酶介导的坏死性蛋白切割。所以,细胞焦亡是由细胞凋亡和细胞坏死来共同执行的死亡形式。
进一步利用识别坏死切割新生末端的抗体ABHD16A-C进行分析,研究人员在LPS/Nigericin诱导的细胞焦亡中观察到至少三类细胞:一类为caspase-3不激活但ABHD16A-C阳性的细胞,代表GSDMD介导的坏死样细胞;一类为caspase-3激活但ABHD16A-C阴性的细胞,代表凋亡细胞;还有一类同时具有两类标志,代表凋亡后的继发性坏死细胞。该结果说明,即使在单一刺激下,不同细胞也可能进入不同死亡轨道,而群体平均信号往往会将这些本质不同的过程混合在一起。
这一发现提示,在研究复杂生理和病理条件下的细胞死亡时,不能仅凭群体水平的总体效应简单定义死亡类型,而需要结合单细胞动态观察和终末标志物识别,重新理解细胞死亡的异质性与层级性。因此,该研究不仅揭示了坏死终末阶段的新机制,也为细胞死亡研究提供了从“群体分类”走向“单细胞命运解析”的新范式。
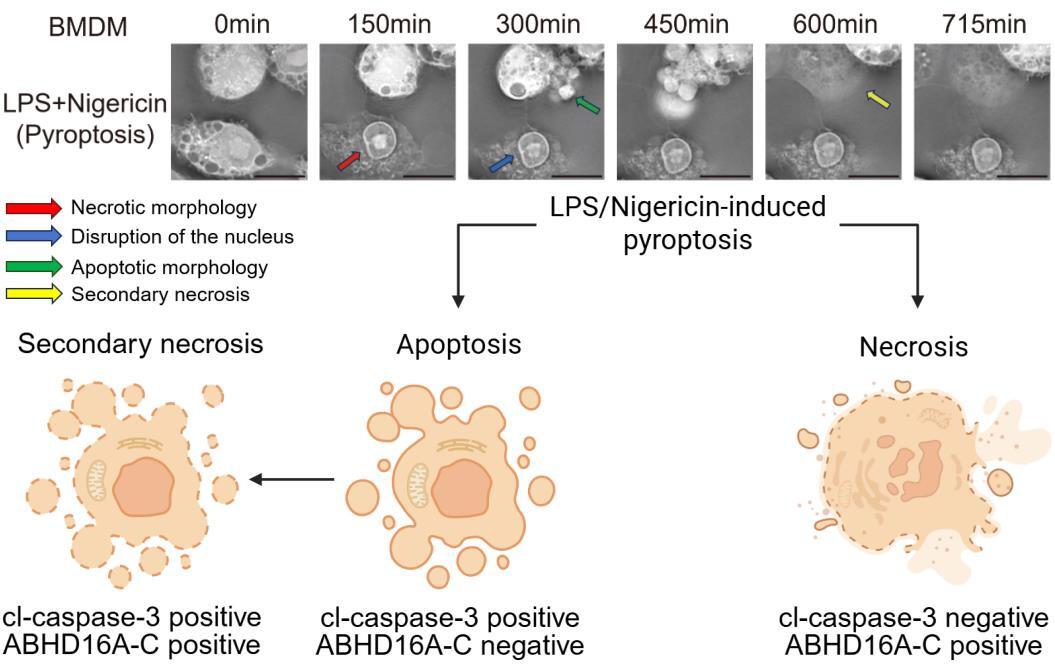
图3. LPS/Nigericin诱导的细胞焦亡中,单细胞层面呈现凋亡与坏死两种死亡方式
论文的通讯作者是中国科学院上海有机化学研究所生物与化学交叉研究中心主任袁钧瑛院士和单冰副研究员。第一作者是中国科学院上海有机化学研究所生物与化学交叉研究中心李甘泉博士。中国科学院上海有机化学研究所生物与化学交叉研究中心张耀阳研究员给N端标记蛋白质谱分析提供了宝贵建议,北京大学施可彬团队对超分辨率ODT显微成像技术的使用和数据分析提供了宝贵帮助,北京大学陈良怡研究员对超分辨率SIM显微成像技术的使用提供了宝贵帮助,上海交通大学医学院附属仁济医院李佩盈研究员提供了宝贵的病人样本。该工作受到了国家自然科学基金、中国科学院先导专项和上海市科委的大力资助。
原文链接:https://www.vita-journal.com/vita/EN/10.15302/vita.2026.04.0023
附件下载: