含氯天然产物因其独特的生物活性一直受到有机合成化学家的广泛关注,同时含氯甾体药物作为一类重要的合成甾体在临床上广泛应用,因此发展高效的合成策略实现含氯甾体分子的简洁、精准合成具有非常重要的研究意义。Clionastatins A和B是2004年由意大利科学家Fattorusso等人从海洋穴居海绵Cliona nigricans中分离出来的一类多氯代甾体天然产物,具有良好的抗肿瘤细胞毒性(IC50 = 0.8-2.0 μg/mL)。它们是首例从自然界中分离出来的多卤代甾体天然产物,且分子中氯原子不以常见的氯醇形式存在。由于分离得到的天然产物量非常少(每个天然产物仅分离得到1 mg左右的样品),其化学结构仅通过核磁谱图确定;同时分离文献中并未报道天然产物的单晶结构和核磁碳谱谱图,而仅是通过二维核磁谱图HSQC和HMBC完成了碳谱化学数据的指定,因此其报道的化学结构和碳谱数据的准确性还需要进一步通过化学合成的手段鉴定。
中国科学院上海有机化学研究所天然产物有机合成化学院重点实验室桂敬汉课题组一直致力于活性甾体和萜类天然产物的高效合成研究,在之前的工作中他们发展了基于骨架可控性重组的仿生合成策略实现了多个复杂甾体天然产物的高效合成(J. Am. Chem. Soc. 2018, 140, 9413; 2019, 141, 5021; 2020, 142, 5007; 2021, 143, 4886; Angew. Chem. Int. Ed. 2021, 60, 11222)。近日,该课题组报道了多氯代甾体天然产物clionastatins A和B的首次全合成并对其结构进行了修正(J. Am. Chem. Soc. 2021, DOI: 10.1021/jacs.1c07511)。基于天然产物结构的分析,他们认为这类天然产物合成的难点在于:1)根据Furst-Plattner规则,即环己烯的双卤代反应倾向于给出双直立键产物,因此clionastatins中处于准平伏键C1和C2双氯原子的立体选择性引入极具挑战;2)分子中存在非常独特、高度不饱和的3,5,8,16-四烯-7,15-双酮结构,易于发生B环的芳构化反应,因此如何选择合适的时机引入B环的不饱和结构同时避免其发生芳构化反应非常重要;3)天然产物报道结构的不确定性大大增加了合成的难度。
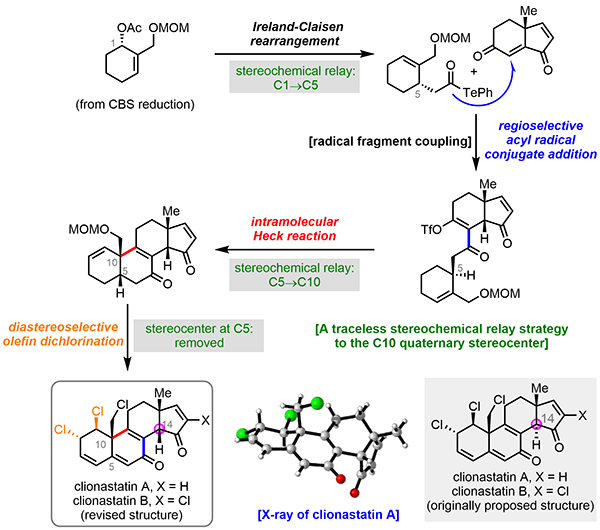
他们从已知烯酮化合物出发,通过CBS还原和Ireland-Claisen重排反应实现了手性酰基自由基前体的制备,并将产生的C1手性立体化学转移至C5位;随后通过酰基自由基共轭加成反应和分子内Heck反应构筑了天然产物核心的四环骨架结构,并将C5手性立体化学转移至C10位,得到了正确构型的C10季碳手性中心;最后通过亚磺酸内酯底物控制的烯烃双氯代反应引入了挑战性的C1和C2准平伏键双氯原子,随后脱氢反应消除C5手性中心,最终他们以16-17步反应完成了clionastatins A 和B的首次全合成。合成样品的NOE谱图和clionastatin A的单晶结构均显示天然产物的C/D环是顺式稠合的方式(即C14-H处于β构型),而不是文献报道的反式稠合的结构(即C14-H处于α构型),因此纠正了文献中错误报道的天然产物结构。值得指出的是,整个合成过程中他们使用了无痕立体化学传递(traceless stereochemical relay)的策略,即由CBS还原反应、Ireland-Claisen重排反应和分子内Heck反应实现了C10位季碳手性中心的精准构建。该工作展示了汇聚式合成策略在复杂天然产物合成中的高效性,同时体现了天然产物合成目前仍是复杂分子结构鉴定或修正的重要手段。
桂敬汉课题组居炜博士和博士研究生王旭东为该论文的共同第一作者。该工作得到了国家自然科学基金委和上海市科委的资助。
图 多氯代甾体天然产物clionastatins A和B的首次全合成