上海有机所交叉中心破解IL-7R跨膜突变致病机理,并实现精准靶向干预
长期以来,膜蛋白的跨膜结构域(TMD)被认为仅起到膜锚定的作用。然而,近年来研究表明,TMD在受体组装、构象耦联及信号转导中具有关键调控功能。在细胞因子受体 (Cytokine receptors) 中,TMD突变常引发异常的、非配体依赖性的激活,并与多种肿瘤的发生发展密切相关,但其分子机制长期未明。
以白细胞介素-7受体(IL-7R)为例,其跨膜区V253G突变已被报道可导致T细胞急性淋巴细胞白血病(T-ALL)。正常情况下,IL-7R需结合配体IL-7并与共受体IL2Rγ (γc) 形成异源二聚体,从而激活下游JAK/STAT信号通路;而V253G突变则绕过这一调控过程,直接诱导JAK1和STAT5的持续激活。
2026年4月29日,中国科学院上海有机化学研究所生物与化学交叉研究中心周界文团队联合德国奥斯纳布吕克大学的Jacob Piehler团队以及浙江大学蔡甜甜团队在Proceedings of the National Academy of Sciences (PNAS)上发表了题为“Structural Rewiring of IL-7R Dimerization by an Oncogenic Transmembrane Mutation Can Be Reversed by Rational Design”的研究论文。该研究系统揭示了这一“隐藏”于跨膜区的突变如何驱动肿瘤发生,并提出了基于结构设计的跨膜多肽精准干预策略。
研究团队综合运用核磁共振(NMR)、分子动力学模拟、生化细胞实验及单分子成像等手段,解析了V253G突变的致病机理。结果表明,该突变使跨膜螺旋的二聚界面发生约170°旋转,从而彻底改变了受体的二聚模式,形成稳定且具备信号激活能力的构象。相比之下,WT IL-7R虽也可形成同源二聚体,但其构象不利于信号传递,表明“二聚构象”而非“是否二聚”才是决定受体激活的关键(图1)。
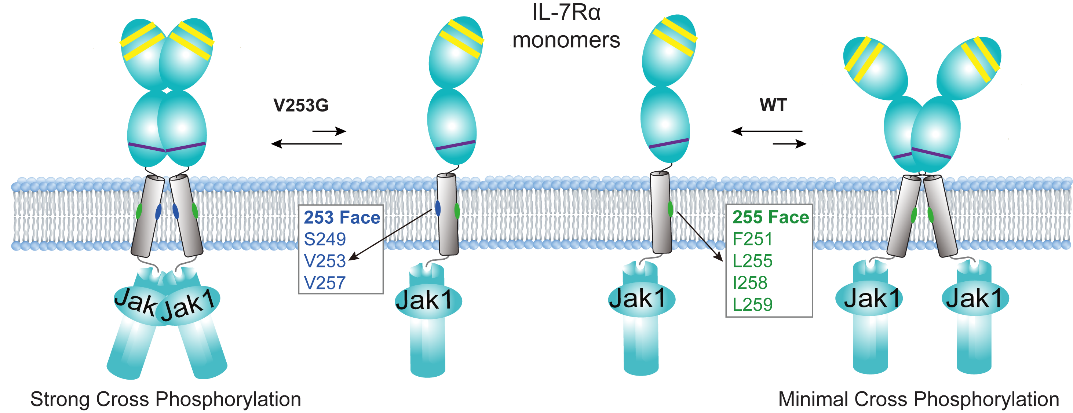
图1. V253G IL-7R激活型同源二聚体与WT IL-7R非激活型同源二聚体的对比。在V253G IL-7R中,S249、V253和I257构成同源二聚界面,从而促进JAK1–JAK1形成有利于交叉磷酸化的配对构象。相比之下,WT IL-7R的同源二聚界面由F251、L255、I258和L259组成,该构象不利于JAK1–JAK1的交叉磷酸化。
基于这一机制,研究人员进一步理性设计了跨膜多肽分子,可特异性干扰突变体形成的异常二聚界面。这些多肽表达基因通过慢病毒或脂质纳米颗粒(LNP)递送进入细胞后,能够有效抑制非配体依赖的异常信号,同时不影响正常的配体依赖性功能,实现了高度特异的调控(图2)。
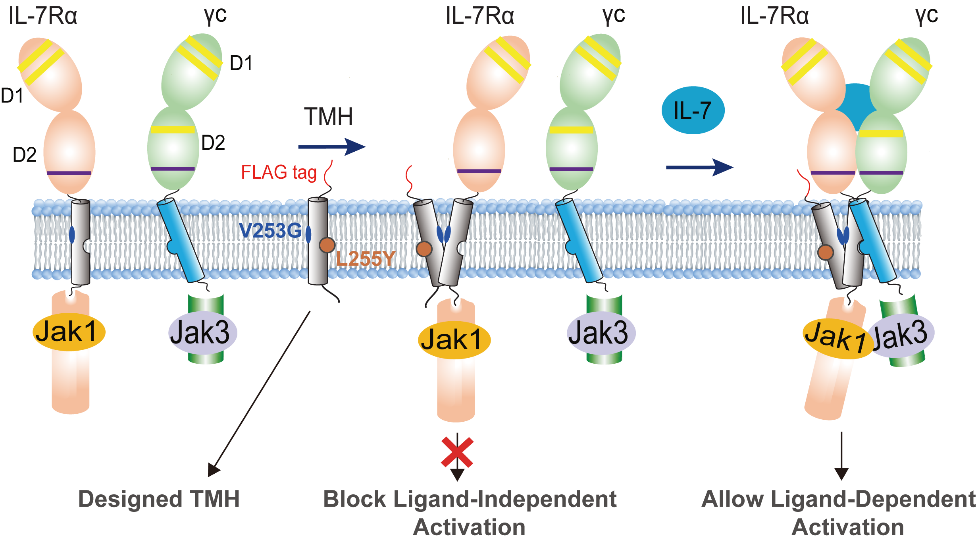
图2. 跨膜多肽设计策略的示意图。通过竞争性阻断IL-7R V253G突变体的同源二聚化,从而抑制非配体依赖的受体激活,同时不影响IL-7诱导的正常信号传导。
该研究不仅阐明了跨膜突变通过改变受体二聚构象从而激活信号的分子机制,也提出了一种针对“不可成药”膜嵌入区域的干预策略。随着mRNA等递送技术的发展,这一基于结构设计的跨膜靶向方法有望拓展至更多由类似突变驱动的疾病,为精准治疗提供新的思路。
中国科学院上海有机化学研究所生物与化学交叉研究中心周界文研究员、德国奥斯纳布吕克大学Jacob Piehler教授和浙江大学量子精密研究院蔡甜甜教授为本文的共同通讯作者。中国科学院上海有机化学研究所生物与化学交叉研究中心博士后王倩、副研究员陈敏以及奥斯纳布吕克大学Asma Lasram为为共同第一作者。以上工作得到了国家自然科学基金委、中国科学院、上海市科委的大力资助和支持。
文章链接:www.pnas.org/doi/10.1073/pnas.2601748123
附件下载: