

自Nicolaou开创性地运用电环化反应合成endiandric acids以来,电环化策略在天然产物全合成中开始引发关注,然而其威力一直未被充分认识。电环化反应的优点在于:1) 具有较强的热力学驱动力和较高的成键/成环效率,无需对成键位点进行预先官能化;2) 容忍多取代底物,取代基立体化学问题预先独立解决;3) 易于采取汇聚式策略构建三烯前体,提高合成的总体效率。但其在复杂分子合成中的弱点在于制备顺式共轭烯烃底物的困难。生命有机化学国家重点实验室李昂课题组着眼于6π电环化在合成多取代六元环方面的优势,将其与环己二烯的氧化芳构化相结合,发展了构建多环体系中多取代芳环的合成策略,在daphenylline, xiamycin A, oridamycins A和B, dixiamycin C, rubriflordilactone A和clostrubin等天然产物的全合成基础上,近期完成了苯并噁唑二萜ileabethoxazole, pseudopteroxazole和seco-pseudopteroxazole的全合成 (Angew. Chem. Int. Ed. DOI: 10.1002/anie.201510568)。该类分子是由Rodríguez等从加勒比海柳珊瑚中分离鉴定的,具有显著的抗结核菌活性。
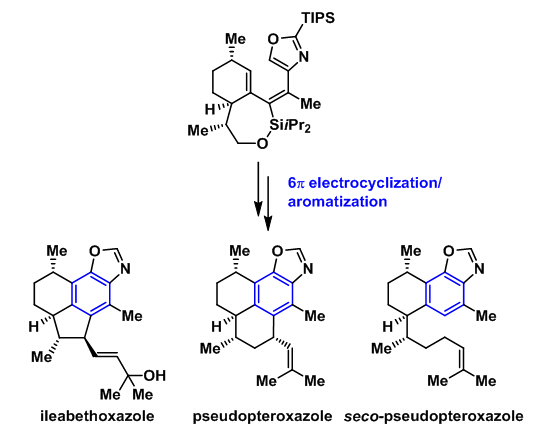
李昂课题组的阳铭博士和阳晓文发展了一种通用性的合成策略:关键六取代三烯中间体的构建依靠串联炔烃碳钯化/Stille反应实现,中间全取代烯烃的几何构型通过顺式的炔烃碳钯化过程得以严格控制;该中间体经过6π电环化/芳构化转化为全取代芳环,作为合成不同分子的共同中间体;芳环上的硅取代基可以灵活地转化为多种官能团,再通过不同的自由基环化反应进行环系的修饰和立体化学的确立,从而获得三个天然产物。合成路线的灵活性为此类分子构效关系的研究提供了可能。该项工作是与中国药科大学孙宏斌教授合作完成的。
该项工作受到科技部973计划青年项目、国家杰出青年基金、国家自然科学基金委优秀青年基金和重大研究计划、中国博士后基金、中组部青年拔尖人才计划、科技部创新人才推动计划、上海市基础研究重大项目和生命有机化学国家重点实验室的大力资助。
附件下载: