

10月11日,《Nature Communications》发表了中国科学院上海有机化学研究所生命有机化学国家重点实验室王婧研究员团队和以色列希伯来大学Ehud Razin教授合作的最新研究成果“第二信使Ap4A在肥大细胞激活过程中多聚化靶向蛋白HINT1行使信号转导功能”。这项工作首次报道了第二信使小分子Ap4A通过诱导靶蛋白HINT1 多聚化,参与过敏反应的分子作用机制。
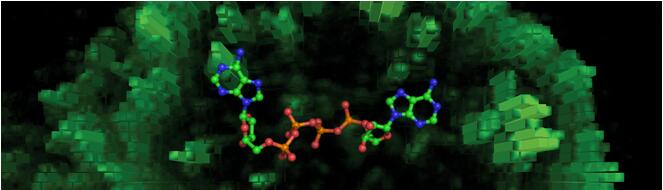
图1. 促进靶向蛋白HINT1发生多聚化的第二信使小分子—Ap4A
肥大细胞(Mast cell,MC)是由髓样干细胞分化形成的一类血液白细胞。肥大细胞广泛分布于生物体-环境界面,比如于皮肤、呼吸道等结缔组织中的血管和毛细血管周围,是发现外源物质的“哨兵”细胞。而肥大细胞的病态激活,则是导致过敏反应发生的主要原因。当肥大细胞受过敏原激活后,细胞内第二信使Ap4A(由4个磷酯键连接两个腺苷所形成的小分子化合物),在30分钟内浓度快速上调5-10倍。Ap4A进而结合下游靶蛋白HINT1,解除HINT1对肥大细胞标志转录因子MITF的抑制作用,释放MITF并激活包括细胞因子受体和多种蛋白酶的转录表达,促进过敏反应的发生。(Mol. Cell, 2013, 10;49(1):30-42; Immunity, 2004, 20(2):145-51;Mol. Cell, 2009, 12;34(5):603-11;Oncogene, 2017, 36(33):4732-4738)。Ap4A如何在分子水平识别HINT1,以及识别之后如何破坏HINT1-MITF相互作用是这个过程中的关键问题。
结合结构生物学,化学生物学和细胞生物学的多种研究方法,该研究小组首次发现在过敏反应中, 第二信使小分子Ap4A通过自身对称的“腺苷”基团聚合靶向蛋白HINT1,由此屏蔽和MITF的识别界面,释放MITF转录活性并促进过敏反应发生的调节机理。这种全新的“链型多聚”作用方式,突破了第二信使小分子依赖“构象变化”对靶蛋白进行调节的传统认识,是信号转导调节模式的一个重要观念更新。
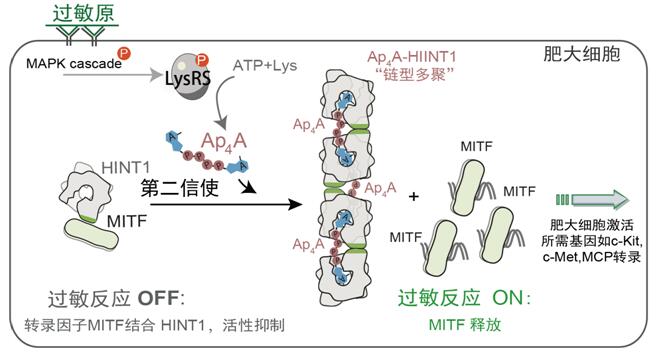
图2. 肥大细胞过敏反应中第二信使Ap4A的调控机理
Ap4A,作为具有药物活力的小分子,直接生理效应包括抗血栓形成、调节血管收缩,已经作为一类眼药水的辅助剂应用到临床。通过从结构生物学,化学生物学角度理解小分子Ap4A与调节蛋白HINT1的相互作用方式,释放肥大细胞标志转录因子MITF活性的分子机制,不仅可以深化对过敏反应中的调控机制的理解,还可以为哮喘等多种过敏疾病的治疗提供新的思路和方法。
上海有机所助理研究员余竞为该论文的第一作者,王婧研究员与以色列希伯来大学Ehud Razin教授为该论文的共同通讯作者。这项工作得到了上海有机所刘聪研究员、康经武研究员,上海科技大学钟桂生研究员等在电镜分析,质谱鉴定方面的大力支持。该研究得到了基金委、中国科学院战略性先导科技专项(B类)及上海市科委的项目资助。
参考资料:
1. Yu J, Liu Z, Liang Y, Luo F, Zhang J, Tian C, Motzik A, Zheng M, Kang J, Zhong G, Liu C, Fang P, Guo M, Razin E, Wang J. Second Messenger Ap4A Polymerizes Target Protein HINT1 to Transduce Signals in FcεRI-activated Mast Cells. Nature communications 10, 4664 (2019).
附件下载: