

平均研发一款新药需要10亿美元和10年的时间,而进入临床试验的药物中有超过90%无法获批上市。如果在新药研发早期能预测疗效和潜在的副作用,就可以避免损耗,提高新药研发的效率。这需要在蛋白组层面无差异化地分析与小分子药物发生相互作用的蛋白质,确定作用靶标。可是,到目前为止这仍然是一个挑战性的工作。
为此,生命过程小分子调控重点实验室康经武课题组提出基于质谱的多组学整合分析的新策略。通过化学蛋白组学,可以全面鉴定小分子药物与蛋白亲和作用的蛋白谱(profiling);通过磷酸化蛋白组学和非靶向代谢组学分析,可以定量揭示药物对细胞过程的扰动事件,包括引起的蛋白表达变化,调控细胞过程的蛋白激酶活性的改变以及代谢网络中的代谢中间产物的变化。高分辨质谱和先进算法获得的大数据在经过统计分析和生物信息学分析后,我们可以找到药物分子扰动细胞过程后留下的痕迹,以及细胞对药物刺激产生响应的分子生物学机制,由此推测出药物的靶标蛋白。通过生物化学、生物物理学和遗传调控学的方法对推测的靶标蛋白进行验证,最终确定药物的作用靶标。
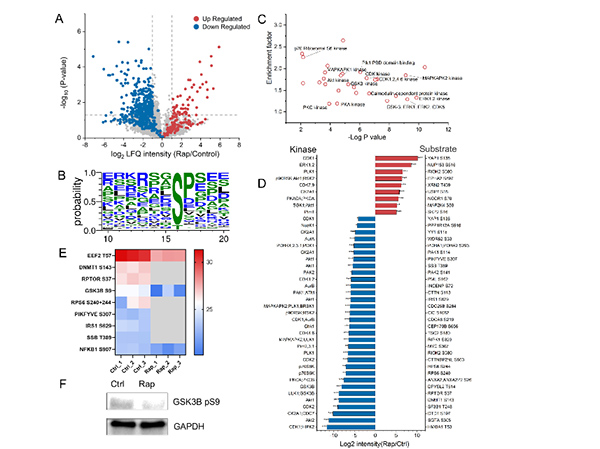
以雷帕霉素(Rap)为例:化学蛋白组学可以鉴定到47种具有高置信度的Rap结合蛋白,包括已知的靶标蛋白FKBP12;磷酸化蛋白质组学分析显示,255个显著性的下调和150个上调磷酸蛋白;非靶向代谢组学分析显示22种显著性下调代谢物和75种上调代谢物。对它们进行功能注释,激酶-底物富集分析,将代谢中间产物映射(mapping)到相应的生化反应途径,进一步的数据的整合分析可以绘制出Rap的作用网络图,从而揭示其参与调节的多个细胞过程的分子机制,如抑制细胞生长、增殖、DNA复制,参与免疫、自噬、程序性细胞和衰老死亡等。这一策略还用于在分子水平揭示和描绘细胞经阿霉素刺激后细胞内发生的一系列响应机制,如修复DNA和线粒体损伤的应急机制。利用这一策略,我们还发现培利替尼作用细胞后,不仅可以抑制酪氨酸激酶活性,还能够诱导乳腺癌细胞中的PRDX4蛋白的发生泛素化-蛋白酶体参与的蛋白降解。
总之,通过基于质谱的多组学整合分析,我们能够在蛋白组层面和分子水平获得前所未有的小分子药物与蛋白(物理和功能)相互作用的信息,为揭示小分子药物复杂的作用机制,预测可能的毒副作用提供依据。这些相互作用信息能够发现新的潜在作用靶标,从而实现老药新用。这一系列的工作分别发表在Anal Chem,2022, 94, 17121; 在线发表在Anal Chem 2023 https://doi.org/10.1021/acs.analchem.3c00867, 以及J Pharm Biomed Anal, 2023, 230, 115398。3篇论文的通讯作者为康经武研究员,第一作者分别为钱珊珊博士、许瑶博士和博士研究生李京同学。本工作受国家自然科学基金、中国科学院先导计划B资助。
附件下载: