

近期,中国科学院上海有机化学研究所生命有机化学国家重点实验室刘文课题组首次阐明了利普斯他汀(Lipstatin)生物合成过程中碳骨架的形成机制(J. Am. Chem. Soc.2019, 141, 3993-4001)。
Lipstatin是从毒三素链霉菌(streptomyces toxytricini)发酵液中分离鉴定的天然产物,具有良好的抑制酯酶的活性。Lipstatin氢化的衍生物Orlistat(奥利司他)是目前FDA唯一批准的治疗肥胖症的非处方药物。虽然Lipstatin具有如此大的价值,但人们对它0的生物合成过程所知甚少。在前期报道的工作中,刘文课题组与上海交通大学陶美凤课题组合作,确定了Lipstatin的生物合成由六个蛋白参与(依次编号为LstA-LstF),并从对应蛋白敲除的突变株中分离鉴定了关键的中间产物(Appl. Environ. Microbiol. 2014, 80, 7473-7483)。他们发现敲除基因簇中两个KAS-III同源蛋白LstA和LstB后,都未在其突变株中检测到有价值的中间产物,说明LstA和LstB可能与Lipstatin的骨架合成相关。在保守催化三联体Cys-His-Asn的作用下,典型的KAS-III通过脱除活性的羧基形成亲核进攻的烯醇式中间体来起始缩合反应。虽然LstA和LstB同属于KAS-III家族,但只有LstA具有保守的催化三联体Cys-His-Asn,而LstB中对应的氨基酸都发生了突变。此结果说明单独的LstA就具备完整的缩合功能,而LstB在Lipstatin骨架合成中又扮演了怎样的角色?
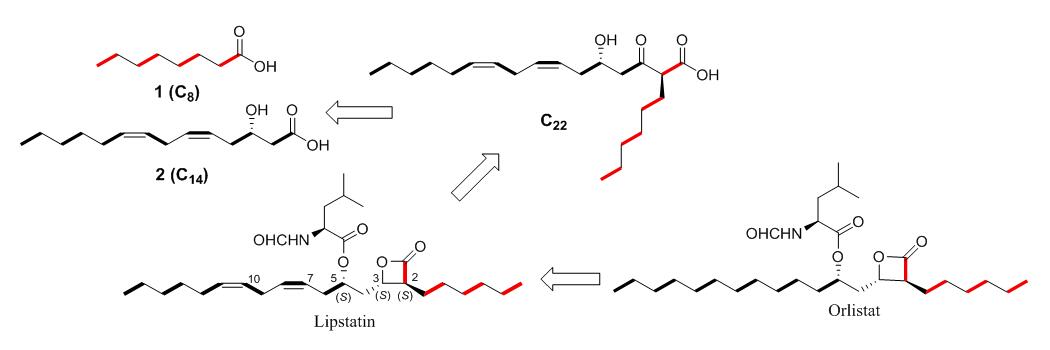
图1 Lipstatin和Orlistat转化关系以及Lipstatin的生物合成反分析。
此次工作中,他们通过体外酶学实验确定了LstA,LstB和LstD在Lipstatin骨架形成中负责的功能。LstA和LstB以特殊的异源二聚体存在,并以非脱羧基式的Claisen缩合反应,协同催化底物间缩合:LstA首先使用保守的半胱氨酸(Cys128α)挂载8碳底物,而用于亲核进攻的烯醇式中间体则经LstB中保守的谷氨酸(Glu60β)催化形成;有趣的是,当使用α,β不饱和双键的8碳底物时,LstAB又催化了另外一种缩合机制,其中关键的烯醇式中间体由Glu60β引发1,4-Micheal加成反应而形成。缩合的中间产物从Cys128α上水解后,再经LstD催化还原,生成羧基更加稳定的还原产物。他们还考察了LstAB对底物的容忍性,发现SNAC、苯硫酯类的模拟底物以及饱和脂肪链和一些双键位移的类似物都能被LstAB接受。KAS-III和它所属的硫解酶超家族蛋白多以同源二聚体的方式催化反应。LstAB新颖催化机制的解析也让人重新审视硫解酶超家族蛋白的功能机制。LstAB的同源蛋白广泛地存在于链霉菌,诺卡氏菌和分枝杆菌等的菌属中,而其负责合成化合物的结构和功能仍待后续揭示。
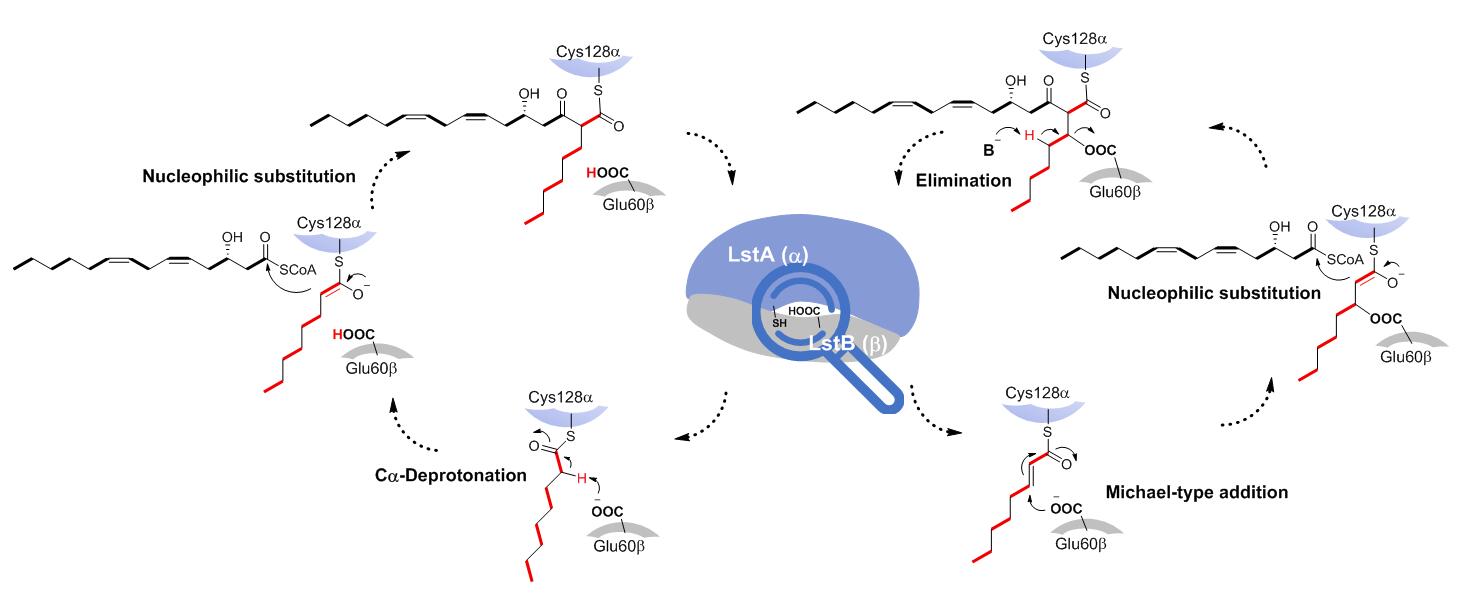
图2 异源二聚体 LstAB催化缩合机制
该工作主要由刘文课题组的张道忠博士完成,获得了国家自然科学基金委,科技部,上海市科委和中科院等相关项目的资助。
附件下载: