研究成果
2020年代表性研究工作进展
代表性研究工作进展
|
代表性工作1 |
名称 |
本实验室固定人员 参加名单 |
所属研究方向 |
|
苯酚衍生物的三氟甲基化反应 |
卿凤翎,徐修华 |
面向世界学科前沿的氟化学基础研究 | |
|
|
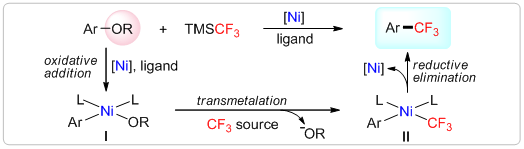
苯酚衍生物的三氟甲基化反应 自从上世纪六十年代起化学家已发展出一系列将三氟甲基引入芳香环的合成方法。这些合成方法可分为如下几类反应:(1)研究最为广泛的芳基碘(溴)化物的三氟甲基化反应;(2)近年来发展出的芳基亲核试剂(如芳基硼酸)的三氟甲基化反应;(3)最近发展的活泼芳基亲电试剂(如芳基重氮盐)的三氟甲基化反应。从这些反应可看出,科学家一直在探索各种芳香底物的三氟甲基化反应。然而令人惊奇的是:尽管近年来通过镍活化苯酚及其衍生物的C-O键后与亲核试剂进行偶联反应已进行广泛研究,但苯酚及其衍生物的三氟甲基化反应一直没有报道。本小组近年来一直致力于发展三氟甲基化新反应(Acc. Chem. Res.2014,47, 1513-1522)和新试剂(Angew. Chem. Int. Ed.2018,57, 6926-6929;Angew. Chem. Int. Ed.2019,58, 10320-10324)。最近成功地实现了镍参与下芳基丙戊酸酯的三氟甲基化反应。 通过对金属参与(催化)芳基底物三氟甲基化反应机理的分析,认为苯酚及其衍生物的三氟甲基化反应具有如下挑战:(1)二价芳基镍络合物(I)与三氟甲基试剂不易发生转金属化形成二价芳基三氟甲基镍络合物(II); (2)二价芳基三氟甲基镍络合物(II)很难发生还原消除反应。如果突破了这二个基元反应,这将发展出一类自然界广泛存在苯酚及其衍生物的三氟甲基化反应。
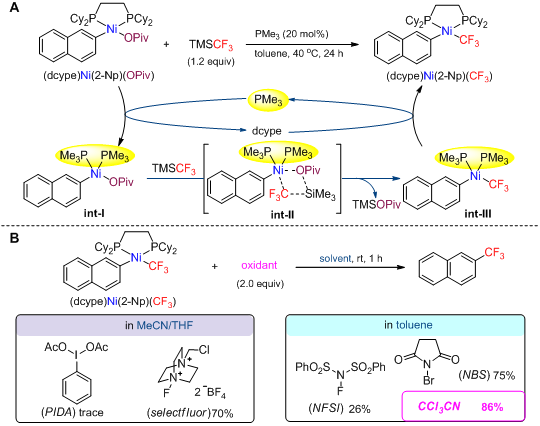
首先,根据文献方法从芳基丙戊酸酯2-NpOPiv合成了二价芳基镍络合物(dcype)Ni(2-Np)(OPiv),并探索它与三氟甲基化试剂TMSCF3的转金属反应,期望得到芳基三氟甲基二价镍络合物(dcype)Ni(2-Np)(CF3)。结果表明,该转金属反应容易生成一些副产物如(dcype)Ni(CF3)(OPiv)和(dcype)Ni(CF3)2。通过对反应中间体的分析和条件筛选,我们找到了最优的转金属反应条件:以甲苯为溶剂并加入催化量的PMe3。机理研究表明,PMe3和dcype的配体交换是促进该转金属反应的关键因素。 接着,对于芳基三氟甲基二价镍络合物(dcype)Ni(2-Np)(CF3)的还原消除展开研究。美国 Melanie S. Sanford教授发现芳基三氟甲基二价镍络合物氧化成高价镍络合物(Ni(III) 或 Ni(IV))可发生还原消除反应得到三氟甲基芳基化合物。因此,对氧化剂进行了探索,发现常用于二价镍络合物的氧化剂并不适应于芳基三氟甲基二价镍络合物。令人惊奇地是,最终发现CCl3CN可以高效地促进(dcype)Ni(2-Np)(CF3)发生还原消除反应生成2-NpCF3。
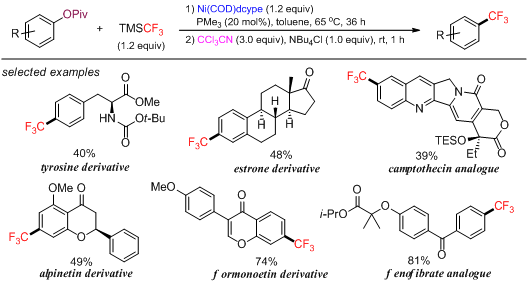
在以上基元反应研究的基础上,本小组通过一锅法实现了一系列芳基丙戊酸酯的三氟甲基化反应,该反应也可应用于一些复杂药物分子的后期三氟甲基化修饰。
该工作发表在 Angewandte Chemie International Edition (2020, 59, 16076),并且被编辑选为 Hot Paper。 | ||
|
代表性工作2 |
名称 |
本实验室固定人员 参加名单 |
所属研究方向 |
|
氟碳链可控延长与光氧化还原产生含氟碳正离子 |
胡金波、倪传法、张伟、何正标 |
面向世界学科前沿的氟化学基础研究 | |
|
|
氟碳链可控延长与光氧化还原产生含氟碳正离子
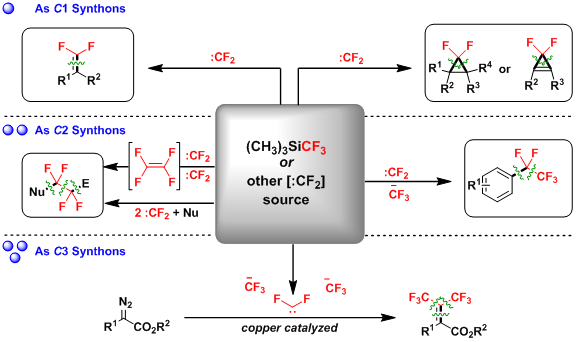
1、氟碳链可控延长 同系化反应(Homologation)在传统有机反应中比较常见,例如Arndt-Eistert反应、Kowalski 反应等,但含氟碳链的同系化延长反应却十分罕见。通常,氟碳链增长通过四氟乙烯的调聚来实现,这种方法不但无法控制氟碳链长度,而且反应过程非常危险。通过CF2的可控插入来精准合成含氟碳链,不但可以突破传统方法的局限,而且对新型含氟功能分子的设计与合成具有重要意义。TMSCF3不但被广泛用作三氟甲基化试剂,而且被胡金波等开发为二氟卡宾试剂(Angew. Chem. Int. Ed. 2011, 50, 7153),并得到广泛应用。其中,TMSCF3所产生的二氟卡宾与烯烃的[2+1]环化反应被称为“Prakash-Hu二氟环丙烷化”(J. Am. Chem. Soc. 2020, 142, 14649)。在过去三年多的时间里,胡金波课题组利用TMSCF3作为含氟碳来源,围绕氟碳链可控延长,先后实现了从C1到C2以及从C1到C3的氟碳链延长反应。
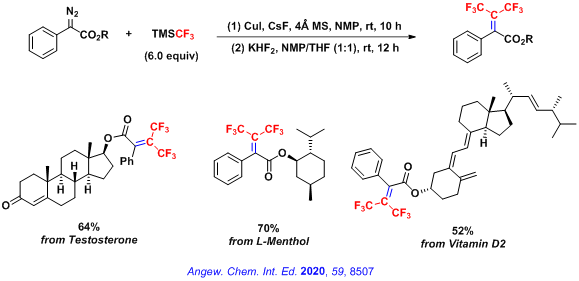
2017年,胡金波课题组利用TMSCF3可以在温和条件先下释放二氟卡宾这一特点,成功实现了在实验室快速小量制备四氟乙烯,并用于五氟乙基化和四氟乙基化反应(Angew. Chem. Int. Ed. 2017, 56, 9971),实现了从TMSCF3出发进行的氟碳链延长反应。在此基础上, 胡金波课题组于2018年发展了从TMSCF3出发,不经四氟乙烯就可以进行的五氟乙基化反应,实现了对各类芳基化合物的五氟乙基化,是目前少有的高效合成五氟乙基化合物的方法之一。该反应通过向三氟甲基亚铜中可控插入一个CF2来实现,不仅为五氟乙基类化合物的合成提供了一种实用可行的方法,还为氟化学中的同系化反应研究开辟了新的思路(Angew. Chem. Int. Ed. 2018, 57, 13211–13215)。 2019年,胡金波课题组利用TMSCF3作为含氟C1源实现了对C6F5Cu可控插入两个CF2产生C6F5CF2CF2Cu这一氟碳链延长反应。C6F5CF2CF2Cu可顺利与(杂)芳基碘代物及烯基碘代物偶联来制备-CF2CF2-桥连的化合物(Chem. Sci. 2020, 11, 276)。与已有的构建-CF2CF2-的方法相比,这一新反应条件温和、底物普适性好,以易得的、应用广泛的、商品化的、环境友好的TMSCF3为CF2来源,为合成含-CF2CF2-片段的双芳基化合物提供了一种简便的方法。 2020年,胡金波课题组在对重氮化合物氟烷基化反应开创性研究的基础上,以TMSCF3为唯一的氟碳来源,以偕二氟烯烃为中间体,发展了对α-重氮酸酯的偕双三氟甲基烯基化反应,实现了偕双三氟甲基烯烃的高效合成,并将其应用于复杂天然产物的衍生化(Angew. Chem. Int. Ed. 2020, 59, 8507)。这一策略借鉴了前期实现的对重氮化合物的偕二氟烯基化这一研究成果(J. Am. Chem. Soc. 2013, 135, 17302),在此基础上一锅法对偕二氟烯烃进行双三氟甲基化,实现了从C1到C3的氟碳链延长。该工作通过底物与含氟碳的反应来启动氟碳链延长,不同于前述工作中所采用的先可控延长氟碳链后偶联的策略,为含氟碳的延长提供了新的研究思路。
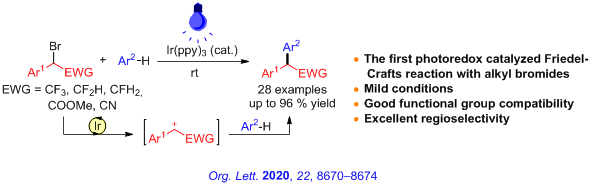
2、光氧化还原产生含氟碳正离子 傅-克(Friedel−Crafts)烷基化反应被广泛用于有机合成,但是,传统方法依赖AlCl3等强Lewis酸来活化卤代烃产生碳正离子进行反应。胡金波课题组发现,缺电子的苄基溴能够在光氧化还原催化下发生两次单电子转移产生苄基碳正离子,继而发生傅-克烷基化反应(Org. Lett. 2020, 22, 8670)。这是首例卤代烃在光氧化还原条件下进行的傅-克反应。反应的成功的关键在于底物要具有于合适的电性。从结果上来看,同时需要苄位有吸电子取代基(促进单电子转移来还原C-Br键产生苄基自由基)和芳环上有电中性或者给电子取代基(促进单电子转移来氧化苄基自由基产生苄基正离子)。该反应条件温和,官能团兼容性高,区域选择性好。与Lewis酸催化体系下的傅克反应进行相比,二者对底物的电性有不同的选择性。Lewis酸催化体系下的傅-克反应优先和富电子C-Br键发生反应,而光氧化还原催化的傅克反应优先和具有一定缺电子性质的底物发生反应。基于这一特点,可以选择性的和其中一个C-Br键进行傅克反应而保留另一个C-Br键。
| ||
|
代表性工作3 |
名称 |
本实验室固定人员 参加名单 |
所属研究方向 |
|
基于氟卤烷烃的催化偶联反应 |
张新刚 |
面向世界学科前沿的氟化学基础研究 | |
|
|
基于氟卤烷烃的催化偶联反应
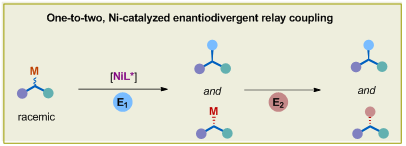
1、对映发散式不对称接力偶联反应(Enatiodivergent Relay Coupling, EDRC) 近年来,镍催化的不对称偶联反应作为一种立体选择性高效构筑碳-碳键的方法受到了化学家们的广泛关注。现已报道的镍催化不对称偶联反应基本是基于手性汇聚的思路。相对于利用消旋亲电试剂进行的催化不对称偶联反应,利用消旋亲核试剂参与的不对称偶联反应研究则鲜有报道,存在很大挑战。主要原因在于诱导消旋亲核试剂生成手性烷基金属中间体是十分困难的。张新刚课题组基于其前期镍催化下氟卤烷烃偶联反应的研究基础,首次提出了对映发散式不对称接力偶联的概念。该策略在手性配体的诱导下,利用镍催化剂立体选择性地拆分消旋亲核试剂中的一种构型底物,并与亲电试剂反应得到光学纯的偶联产物,但另一构型的亲核试剂在该步反应中不受影响。随后,加入第二组份亲电试剂捕获第一步反应后剩余的另一构型亲核试剂,从而可以生成具有不同取代,构型相反的产物。与传统的镍催化手性汇聚式合成方法相比,该策略的特点在于能够实现从单一消旋底物出发合成两种具有不同取代,构型相反的手性化合物,具有高效简洁,手性产物多样的特点。
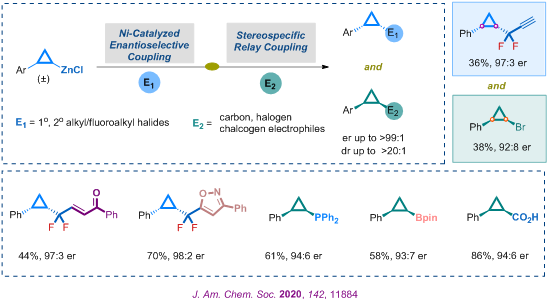
应用这一概念,张新刚课题组首次实现了镍催化下消旋环丙基锌试剂与1级、2级(氟代)烷基卤代物的不对称偶联反应。尤为重要的是对于具有连续四个手性中心的手性三元环结构,该反应依然可以取得优良的产率和高立体选择性。该反应可以“一锅法”对映发散式合成具有不同构型、不同取代的手性三元环化合物,是首例过渡金属催化下基于氟卤烷烃的不对称二氟烷基化反应。该反应所得手性三元环产物可以进行多样性转化,从而可以实现手性三元环化合物的发散式合成,得到一系列含氟手性三元化合物和其他非氟手性化合物,为过渡金属催化的不对称偶联反应提供了新思路。
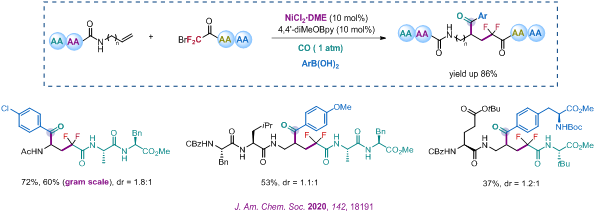
2、 镍催化下螯合基团辅助的烯烃四组分插羰串联反应 2016年,张新刚课题组首次提出了镍催化下螯合基团辅助的烯烃双碳化新型反应策略(Angew. Chem. Int. Ed. 2016, 55, 12270),引发了国际相关领域的研究热点。基于该策略以及该课题组发展的镍催化下氟卤烷烃的插羰反应(Org. Lett. 2019, 21, 1031),他们又首次实现了1大气压CO氛围下,螯合基团辅助的镍催化下烯烃四组分插羰串联氟烷基化反应(J. Am. Chem. Soc. 2020, 142, 18191),是首例镍催化下的四组分插羰反应。镍催化下利用CO的插羰反应一直是个挑战,原因在于镍在CO的氛围中容易形成剧毒的惰性物种Ni(CO)4,该物种会抑制催化循环的顺利发生。然而,张新刚课题组发展的该反应却可以在CO氛围中,将烯烃、芳基硼酸和二氟烷基溴代物高效组合起来,生成串联插羰产物。该反应兼容一系列烯胺、烯丙基胺(醇)和高烯丙基胺(醇)类烯烃,具有优秀的官能团兼容性。尤为重要的是利用该反应可以一步合成含氟五肽化合物,镍催化剂不受毒化,体现了该策略的高效性和实用性。并且,利用所引入的羰基,他们还实现了生物素对多肽的修饰,表明了该反应在化学生物学中的应用潜力。
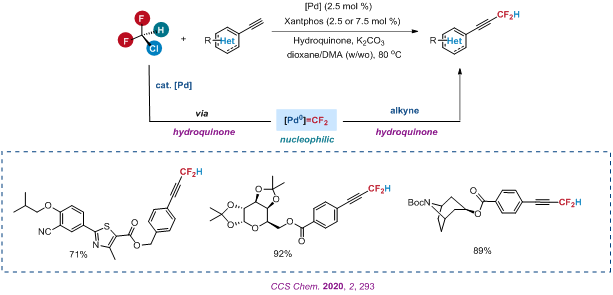
3、 钯二氟卡宾参与的炔烃催化偶联反应 基于张新刚课题组发展的金属二氟卡宾参与的催化偶联反应(Org. Lett. 2016, 18, 44; Nat. Chem. 2017, 9, 918; Nat. Chem. 2019, 11, 948),该课题组利用大宗工业化学品ClCF2H为二氟卡宾前体又实现了钯二氟卡宾参与的炔烃催化偶联反应,对一系列端炔化合物完成了高效二氟甲基化。该反应可以避免传统Sonogashira偶联反应中,由于大部分氟卤烷烃会与零价钯Pd(0)发生单电子转移反应产生氟烷基自由基,进而抑制催化循环,生成含氟烯烃的弊端,代表了一种新的炔烃参与的催化偶联模式。同时,通过详细的机理研究,他们还阐释了添加剂对苯二酚在催化循环中的具体作用(作为质子穿梭载体,调控二氟卡宾的生成速率,以及活性配体的前体),为后续发展新的高效钯二氟卡宾参与的催化偶联反应奠定了基础。
| ||
|
代表性工作4 |
名称 |
本实验室固定人员 参加名单 |
所属研究方向 |
|
首例中性五配位三价铜络合物的分离、鉴定及其C(sp3)-CF3还原消除反应研究、首例可应用于[18F]-标记的二氟甲硫基试剂的创制及反应研究、高反应活性的基于硫/硒叶立德骨架的亲电一氟甲基/三氟甲基化试剂的反应研究 |
沈其龙 |
面向世界学科前沿的氟化学基础研究 | |
|
|
1、 首例中性五配位三价铜络合物 [(bpy)Cu(CH3)(CF3)2]的分离、鉴定及其C(sp3)-CF3还原消除反应研究。铜介导或催化的偶联反应是构建碳碳键的重要方法之一。然而对于铜催化的偶联反应的机理特别是大家普遍认为的三价铜中间体的结构及其基元反应几乎一无所知。我们成功地合成了首例非刚性骨架配体稳定的中性五配位三价铜络合物 [(bpy)Cu(CH3)(CF3)2],并对其结构做了核磁、元素分析及单晶的表征。在50 oC下,该络合物发生C(sp3)-CF3还原消除反应高产率生成三氟乙烷。机理研究包括动力学、DFT计算表明该还原消除反应是一个协同成键的过程。 2、 首例可应用于[18F]-标记的二氟甲硫基试剂的创制及反应研究。正电子断层扫描成像(PET)是目前最先进的用于诊断的成像技术之一。该技术的核心是高效合成放射性的[18F]-标记的示踪剂。我们发展了首例可应用于[18F]-标记的二氟甲硫基试剂PhSO2SCHClF, 系统研究了其与一系列芳基硼化物的反应,并与牛津大学的Gouverneur课题组合作,利用[18F]-KF进行氟/氯交换,高放射收率地合成了[18F]-标记的二氟甲硫基化合物。 3. 高反应活性的基于硫/硒叶立德骨架的亲电一氟甲基/三氟甲基化试剂的反应研究。我们对先前合成的基于基于硫叶立德骨架的亲电一氟甲基试剂的进行了系统的结构-活性相关研究,发展了2个活性更高的亲电一氟甲基化试剂,其与一系列亲核底物的反应均可在室温下20分钟内完成。同时,我们对基于硒叶立德骨架的亲电三氟甲基化试剂的反应进行了进一步研究,发现在Lewis酸Sc(OTf)3与光催化剂的协同作用下,可以发生高效的烯烃三氟甲基化官能团化反应。 | ||
|
代表性工作5 |
名称 |
本实验室固定人员 参加名单 |
所属研究方向 |
|
Separation-free Enantiodifferentiation with Chromatogram-like Output |
赵延川 |
面向世界学科前沿的氟化学基础研究 | |
|
|
手性分子广泛应用于医药、材料及生命等领域,快速确定手性样品的组成对手性相关科学的发展极为重要。目前最常用的手性色谱分析技术基于分离,相对耗时,难于满足高通量手性分析的需求。基于光谱方法(比如圆二色光谱)可以避免分离,实现原位快速分析,但分析准确性易受微量杂质的干扰。色谱方法的“高精确性”和光谱方法的“原位及快速性”是分析领域一直追寻的优良检测特性,然而却难于整合在同一种分析技术中。我们设计了一系列基于手性铝络合物的含氟核磁探针分子。这些探针分子具有空间受限的手性识别空腔,与手性分析物相互作用时可以产生类似色谱峰的特征氟谱信号用于进行手性区分检测。该方法在原位快速检测的前提下,实现了类似色谱方法的高精确性。该方法可以对醇、酰胺、环醚、亚砜等大量结构不同的手性化合物进行快速分析并且实现不同种类手性物质的同时检测。当使用具有自动进样功能的核磁共振波谱,该方法在一天内可以完成超过1000个样品的手性分析,满足高通量筛选的测试需求。此外,利用特征氟谱检测信号可以对手性分子的绝对构型进行快速判断,为液体及非晶样品的构型确定提供新的途径。该方法快速无创的特点及多组分同时分析能力使其有望应用于复杂生命体系中手性物质的原位检测。 | ||
附件下载: